高中化學
-
【觀念】利用物理性質的鑑定方法
-
【觀念】利用化學性質的鑑定方法
-
【觀念】物質鑑定的應用
-
【觀念】水狀態的變化與加熱曲線
-
【觀念】反應熱與熱化學反應式
-
【觀念】常見的反應熱種類(燃燒熱與生成熱)
-
【觀念】赫士定律
-
【觀念】赫士定律的應用
-
【實驗】反應熱的測量
-
【觀念】物質三態的粒子模型
-
【觀念】氣體的通性
-
【觀念】氣體壓力的測量
-
【複習】水狀態的變化與加熱曲線
-
【觀念】波以耳定律
-
【觀念】查理-給呂薩克定律
-
【觀念】亞佛加厥定律
-
【觀念】理想氣體方程式
-
【觀念】理想氣體方程式的應用
-
【觀念】理想氣體與真實氣體差異
-
【觀念】道耳頓分壓定律
-
【延伸】收集氣體的方式
-
【延伸】排水集氣法與氣體壓力校正
-
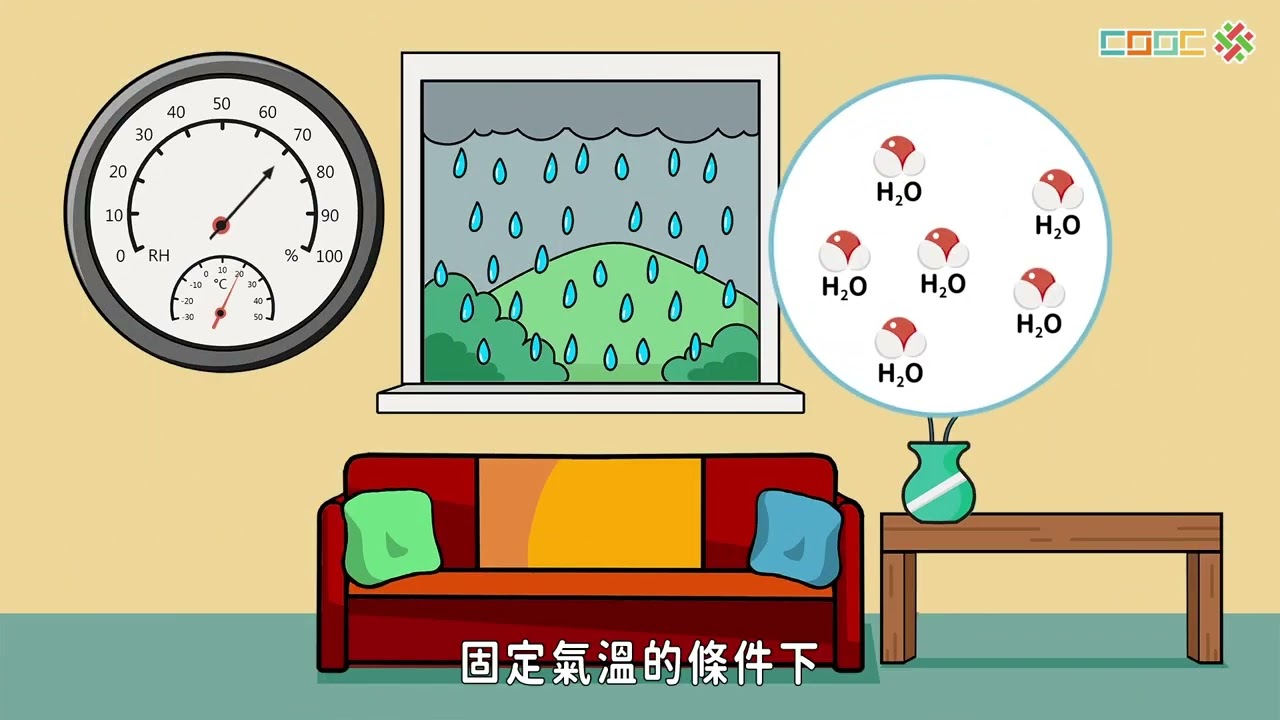
【觀念】水的飽和蒸氣壓與相對溼度
-
【延伸】莫耳分率與重量莫耳濃度
-
【觀念】拉午耳定律-非揮發性溶質溶液的蒸氣壓變化
-
【觀念】拉午耳定律-揮發性溶質溶液的蒸氣壓變化
-
【觀念】氣體溶解度與亨利定律
-
【觀念】理想溶液與非理想溶液
-
【觀念】溶液的沸點變化
-
【觀念】非電解質溶液的凝固點下降
-
【觀念】溶液的依數性質
-
【延伸】電解質的依數性質
-
【實驗】理想溶液與非理想溶液的體積差異
-
【實驗】凝固點下降的現象
-
【觀念】滲透壓
-
【觀念】滲透壓的應用與逆滲透
-
【複習】電磁波、光的二元性與光譜
-
【觀念】氫原子光譜與芮得柏方程式
-
【複習】原子模型的演進
-
【觀念】波耳氫原子模型-1
-
【觀念】波耳氫原子模型-2
-
【觀念】氫原子模型與氫原子光譜
-
【觀念】軌域與量子數
-
【觀念】電子組態的填入規則
-
【觀念】電子組態與週期表
-
【觀念】原子半徑與離子半徑
-
【觀念】游離能
-
【觀念】電負度
-
【觀念】化學鍵-離子鍵及離子化合物的性質
-
【延伸】離子鍵的晶格能
-
【觀念】價鍵理論與共價鍵的形成
-
【觀念】路易斯結構與共振
-
【觀念】價殼層電子對互斥原理與分子形狀1
-
【延伸】價殼層電子對互斥原理與分子形狀2
-
【觀念】混成軌域1
-
【延伸】混成軌域2
-
【觀念】多重鍵的形成
-
【觀念】氫鍵
-
【觀念】氫鍵的影響
-
【觀念】各種晶體的比較
-
【觀念】鍵長、鍵能與鍵級
-
【觀念】共價網狀固體
-
【觀念】極性分子與非極性分子
-
【觀念】分子間的作用力(1)
-
【觀念】分子間的作用力(2)
-
【觀念】σ鍵與π鍵
-
【觀念】金屬鍵及金屬的性質
-
【延伸】晶格堆積
-
【觀念】反應速率的定義
-
【觀念】反應速率的測定
-
【觀念】反應速率定律式簡介
-
【觀念】級數的測定
-
【觀念】零級反應
-
【觀念】一級反應
-
【觀念】半生期的應用
-
【觀念】碰撞學說
-
【觀念】反應位能圖
-
【延伸】反應機構
-
【觀念】反應速率的快慢比較
-
【實驗】秒表反應
-
【觀念】影響反應速率-溫度
-
【觀念】影響反應速率-催化劑
-
【觀念】影響反應速率-濃度與壓力
-
【觀念】影響反應速率-接觸面積
-
【觀念】可逆反應
-
【觀念】動態平衡與平衡常數
-
【觀念】平衡常數的意義與平衡常數表示法
-
【觀念】平衡常數表示法與簡化
-
【觀念】平衡常數與反應式的關係
-
【觀念】勒沙特列原理應用-哈伯法
-
【觀念】實驗:平衡常數的測定
-
【觀念】實驗:勒沙特列原理二氧化氮雙聚反應
-
【觀念】勒沙特列原理-溫度
-
【觀念】勒沙特列原理-濃度
-
【觀念】勒沙特列原理-壓力1
-
【觀念】勒沙特列原理-壓力2
-
【觀念】平衡常數的應用
-
【觀念】沉澱反應的應用
-
【觀念】溶解度與溶度積的關係
-
【觀念】離子積與沉澱反應
-
【觀念】同離子效應
-
【觀念】溶解平衡與溶度積
-
【延伸】沉澱滴定
-
【複習】阿瑞尼斯的酸鹼理論與酸鹼理論的演進
-
【觀念】布忍斯特-洛瑞酸鹼理論
-
【觀念】酸鹼性的強弱
-
【觀念】鹽的種類與名稱
-
【延伸】酸式鹽的酸鹼性
-
【觀念】緩衝溶液的酸鹼度
-
【練習】酸鹼素養試題
-
【複習】氧化還原反應
-
【觀念】法拉第電解定律
-
【觀念】電鍍與其應用
-
【實驗】有電電鍍與無電電鍍
載入中...
相關課程